Triazan
| Triazan | |
|---|---|
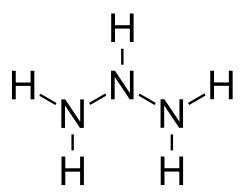 Strukturní vzorec | |
| Obecné | |
| Systematický název | triazan |
| Ostatní názvy | aminohydrazin |
| Anglický název | triazane |
| Německý název | Triazan |
| Sumární vzorec | N3H5 |
| Identifikace | |
| Registrační číslo CAS | 14451-01-5 |
| PubChem | 446953 |
| SMILES | NNN |
| InChI | InChI=1S/H5N3/c1-3-2/h3H,1-2H2 |
| Vlastnosti | |
| Molární hmotnost | 47,059 7 g/mol |
Některá data mohou pocházet z datové položky. | |
Triazan , také nazývaný aminohydrazin je anorganická sloučenina se vzorcem NH2NHNH2, zapisovaným rovněž jako N3H5. Triazan je třetí nejjednodušší azan po amoniaku a hydrazinu. Lzte jej vyrobit z hydrazinu, ovšem je nestabilní a nemůže být izolován v čisté podobě, pouze ve formě solí jako je triazanium sulfát. Pokusy převést triazaniové soli na volnou zásadu měly za následek pouze vznik diazenu a amoniaku.[1] Triazan byl poprvé připraven jako ligand v komplexním iontu stříbra.
Sloučeniny obsahující triazanovou kostru
Je známo několik sloučenin obsahujících triazan jako základ molekuly, například 1-methyl-1-nitrosohydrazin, jenž se vyrábí reakcí bez použití rozpouštědel z methylhydrazinu a alkylnitritu:
CH3NHNH2 + RNO2 → CN3H5O + RHO
1-methyl-1-nitrosohydrazin je bezbartvá kapalina oproti trinitrotoluenu citlivější na náraz, ale méně citlivá na tření; taje při 45 °C a rozkládá se při 121 °C.
Odkazy
Související články
Externí odkazy
 Obrázky, zvuky či videa k tématu Triazan na Wikimedia Commons
Obrázky, zvuky či videa k tématu Triazan na Wikimedia Commons
Reference
V tomto článku byl použit překlad textu z článku Triazane na anglické Wikipedii.