Oxid železnato-železitý
| Oxid železnato-železitý | |
|---|---|
 | |
| Obecné | |
| Systematický název | Oxid železnato-železitý |
| Anglický název | Iron(II,III) oxide |
| Německý název | Eisen(II,III)-oxid |
| Sumární vzorec | Fe3O4 |
| Vzhled | černý ferimagnetický prášek |
| Identifikace | |
| Registrační číslo CAS | 1317-61-9 |
| PubChem | 16211978 |
| ChEBI | 50821 |
| Vlastnosti | |
| Molární hmotnost | 231,539 g/mol |
| Teplota tání | 1 597 °C |
| Teplota varu | 2 623 °C[1] |
| Teplota změny krystalové modifikace | 625 °C (α → β) |
| Hustota | 5,195 g/cm³ (20 °C) |
| Index lomu | nD= 2,42 |
| Tvrdost | 6 |
| Rozpustnost ve vodě | nerozpustný |
| Rozpustnost v polárních rozpouštědlech | kyseliny (reaguje) |
| Součinitel tepelné vodivosti | 1,2–2,5 W m−1 K−1 |
| Struktura | |
| Krystalová struktura | krychlová |
| Hrana krystalové mřížky | a=840 pm |
| Termodynamické vlastnosti | |
| Standardní slučovací entalpie ΔHf° | −1 118 kJ/mol |
| Entalpie tání ΔHt | 576 J/g |
| Entalpie změny modifikace ΔHα→β | 0 J/g |
| Standardní molární entropie S° | 146 J K−1 mol−1 |
| Standardní slučovací Gibbsova energie ΔGf° | −1 015 kJ/mol |
| Izobarické měrné teplo cp | 0,619 J K−1 g−1 |
| Bezpečnost | |
| R-věty | žádné nejsou |
| S-věty | žádné nejsou |
Některá data mohou pocházet z datové položky. | |
Oxid železnato-železitý, chemickým vzorcem Fe3O4 (FeIIO−II·Fe2IIIO3−II), je sloučenina železa a kyslíku. V přírodě se vyskytuje jako minerál magnetit. Je ferimagnetický do teploty 570 °C, nad touto teplotou se stává paramagnetickým.
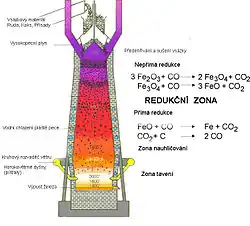
Používá se při výrobě železa ve vysoké peci. Do horní části pece se přidají rudy železa (např. magnetit a hematit) společně s vápencem a koksem. Reakcí koksu se vzdušným kyslíkem, který je do pece přiháněn spodní částí, vznikne oxid uhelnatý, pomocí kterého probíhá nepřímá redukce rud. Dochází k reakci:
- Fe3O4 + CO → 3 FeO + CO2
Vznikající oxid železnatý sestupuje do nižší části vysoké pece, kde je redukován pomocí koksu na železo. Vznikající oxid uhličitý reaguje s koksem za vzniku dvou molekul oxidu uhelnatého, které dále redukují rudy železa.
Reference
- ↑ BLANEY, Lee. Magnetite (Fe3O4): Properties, Synthesis, and Applications [online]. 2007 [cit. 2023-10-21]. S. 77. Dostupné online.
Literatura
- VOHLÍDAL, Jiří; ŠTULÍK, Karel; JULÁK, Alois. Chemické a analytické tabulky. 1. vyd. Praha: Grada Publishing, 1999. ISBN 80-7169-855-5.
Externí odkazy
 Obrázky, zvuky či videa k tématu oxid železnato-železitý na Wikimedia Commons
Obrázky, zvuky či videa k tématu oxid železnato-železitý na Wikimedia Commons