Kyselina fluoroantimoničná
| Kyselina fluoroantimoničná | |
|---|---|
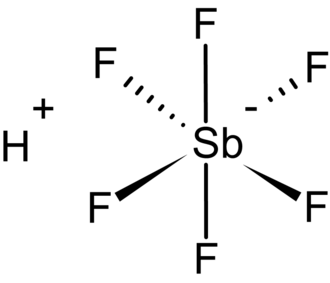 Strukturní vzorec | |
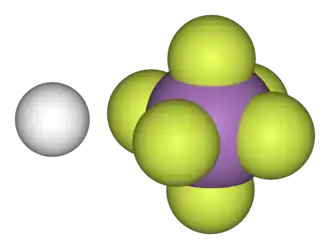 Model molekuly | |
| Obecné | |
| Systematický název | Kyselina fluoroantimoničná |
| Anglický název | Fluoroantimonic acid |
| Německý název | Fluor-Antimonsäure |
| Funkční vzorec | HSbF6 |
| Sumární vzorec | HSbF6 |
| Vzhled | Bezbarvá kapalina |
| Identifikace | |
| Registrační číslo CAS | 16950-06-4 |
| EC-no (EINECS/ELINCS/NLP) | 241-023-8 |
| PubChem | 21953576 |
| SMILES | F[Sb](O)(O)=O |
| Vlastnosti | |
| Molární hmotnost | 236,808 g/mol |
| Teplota varu | rozklad |
| Disociační konstanta pKa | −25 [zdroj?] |
| Rozpustnost ve vodě | vybuchuje |
| Rozpustnost v polárních rozpouštědlech | rozpustná v oxidu siřičitém |
| Bezpečnost | |
 GHS05  GHS06  GHS07  GHS03 | |
| R-věty | R26, R29, R35 |
| NFPA 704 |  0
4
4
|
| Teplota vzplanutí | nehořlavá |
Některá data mohou pocházet z datové položky. | |
Kyselina fluoroantimoničná (HSbF6), taktéž nazývaná kyselina hexafluoroantimoničná, je druhou nejsilnější známou kyselinou (silnější je pouze helonium) a řadí se mezi superkyseliny (je asi 2×1019krát silnější než koncentrovaná kyselina sírová).[2] Její hodnotou H0 je −31,3.
Kyselina fluoroantimoničná se může přechovávat pouze v nádobách z teflonu, které jako jediné nedokáže rozleptat.
Reakce vzniku kyseliny fluoroantimoničné:

Reference
V tomto článku byl použit překlad textu z článku Fluoroantimonic acid na anglické Wikipedii.
- ↑ Safety Data Sheet
- ↑ Superacids. Chemistry LibreTexts [online]. 2015-06-17 [cit. 2023-08-23]. Dostupné online. (anglicky)
Externí odkazy
 Obrázky, zvuky či videa k tématu kyselina fluoroantimoničná na Wikimedia Commons
Obrázky, zvuky či videa k tématu kyselina fluoroantimoničná na Wikimedia Commons
Portály: Chemie