Kyselina chloromravenčí
| Kyselina chloromravenčí | |
|---|---|
 Vzorec | |
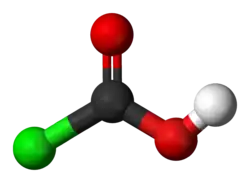 Model | |
| Obecné | |
| Systematický název | Kyselina chloromravenčí |
| Ostatní názvy | Kyselina chloromethanová |
| Sumární vzorec | CClHO2 |
| Vzhled | bezbarvá kapalina |
| Identifikace | |
| Registrační číslo CAS | 463-73-0 |
| Vlastnosti | |
| Molární hmotnost | 80,47 g/mol |
| Rozpustnost ve vodě | Reaguje (na HCOOH a HCl) |
Některá data mohou pocházet z datové položky. | |
Kyselina chloromravenčí (někdy též kyselina chloromethanová) je kapalná, organická látka se vzorcem CClHO2. Jedná se o chlorderivát kyseliny mravenčí, kde je vodík (jediný, nepočítaje ten v -COOH skupině) nahrazen atomem chloru.
Výroba
Tato látka se vyrábí chlorací kyseliny mravenčí, dle rovnice:
HCOOH + 2Cl2 → ClCOCl + 2HCl
Reakce probíhá za zvýšené teploty. Tato látka je pak kontaminována chloridem kyseliny mravenčí. Dále je potřeba provést hydrataci (reakci s vodou):
ClCOCl + H2O → ClCOOH + HCl
Hydrolýza se provádí opatrně, aby se nezničil finální produkt. Produkt se dále čistí destilací.
Reakce
Kyselina chloromravenčí reaguje s vodou za vzniku kyseliny mravenčí a kyseliny chlorovodíkové, dle rovnice:
ClCOOH + H2O → HCOOH + HCl
Proto musí být látka chráněna i před vzdušnou vlhkostí. Reakce je exotermní.
Kyselina chlormravenčí se používá jako karboxylační činidlo. Za přítomnosti Lewisovy kyseliny (nejčastěji chloridu hlinitého) se na molekulu uhlovodíku připojí -COOH skupina.
R-CH3 + ClCOOH —AlCl3→ R-CH2-COOH + HCl
Externí odkazy
 Obrázky, zvuky či videa k tématu kyselina chloromravenčí na Wikimedia Commons
Obrázky, zvuky či videa k tématu kyselina chloromravenčí na Wikimedia Commons