Dikyan
| Dikyan | |
|---|---|
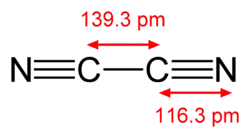 Strukturní vzorec | |
 3D vzorec | |
| Obecné | |
| Systematický název |
|
| Ostatní názvy | dikyan, EDN |
| Anglický název | Cyanogen |
| Německý název | Dicyan |
| Funkční vzorec | (CN)2 |
| Sumární vzorec | C2N2 |
| Vzhled | bezbarvý plyn nebo kapalina |
| Identifikace | |
| Registrační číslo CAS | 460-19-5 |
| EC-no (EINECS/ELINCS/NLP) | 207-306-5 |
| PubChem | 9999 |
| ChEBI | 29308 |
| UN kód | 1026 |
| Číslo RTECS | GT1925000 |
| Vlastnosti | |
| Molární hmotnost | 52,035 g/mol |
| Teplota tání | −27,9 °C |
| Teplota varu | −20,7 °C |
| Hustota | 0,953 7 g/cm³ (−21 °C) 0,002 335 g/cm³ (20 °C) |
| Dynamický viskozitní koeficient | 0,009 28 cP (0 °C) 0,009 87 cP (17 °C) 0,012 71 cP (100 °C) |
| Index lomu | nD= 1,000 82 (0 °C) |
| Kritická teplota Tk | 126,6 °C |
| Kritický tlak pk | 6 009 kPa |
| Rozpustnost ve vodě | 450 ml/100 g (20 °C) |
| Rozpustnost v polárních rozpouštědlech | ethanol 230 ml/100 g (80 °C) |
| Rozpustnost v nepolárních rozpouštědlech | diethylether 500 ml/100 g (18 °C) |
| Van der Waalsovy konstanty stavové rovnice | a= 0,776 9 Pa m6 mol−2 b= 69,01×10−6 m3 mol−1 |
| Ionizační energie | 13,6 eV |
| Struktura | |
| Dipólový moment | 0 Cm |
| Termodynamické vlastnosti | |
| Standardní slučovací entalpie ΔHf° | 308,15 kJ/mol |
| Standardní molární spalná entalpie ΔH°sp | −1 087,7 kJ/mol |
| Entalpie tání ΔHt | 156 J/g |
| Entalpie varu ΔHv | 448,3 J/g |
| Standardní molární entropie S° | 241,8 J−1 mol−1 |
| Standardní slučovací Gibbsova energie ΔGf° | 197,35 kJ/mol |
| Izobarické měrné teplo cp | 1,092 J K−1 g−1 |
| Bezpečnost | |
 GHS02  GHS06  GHS09 Nebezpečí[1] | |
| R-věty | R11, R23, R50/53 |
| S-věty | (S1/2), S23, S45, S60, S61 |
| NFPA 704 |  4
4
2
|
Některá data mohou pocházet z datové položky. | |
Dikyan je jednou z několika kyanových sloučenin. Tyto sloučeniny se vyznačují buď jednomocným zbytkem –CN nebo aniontem CN−. Volný radikál nemůže ovšem existovat, ale je známa sloučenina dikyan, jejíž vzorec je (CN)2. Atomy uhlíku jsou v ní spojeny trojnými vazbami s atomy dusíku.
Vlastnosti
Dikyan je jedovatý plyn, který voní po hořkých mandlích. Jeho teplota varu je -20,7 °C. Dobře se rozpouští ve vodě a v ethanolu. Jeho spalováním za zvýšeného tlaku s kyslíkem lze dosáhnout namodralého plamene, jehož teplota je asi 4 800 °C (s ozónem pak ještě lehce vyšší). Dikyan je tak uváděn jako plyn s druhou nejvyšší teplotou hoření (po dikyanoacetylenu).
Příprava
Nejsnadněji se dikyan připravuje reakcí koncentrovaných roztoků síranu měďnatého a kyanidu draselného, přičemž v první fázi přípravy vzniklý kyanid měďnatý se v druhé fázi samovolně rozloží:
1. Cu2+ + 2CN− → Cu(CN)2
2. 2Cu(CN)2 → 2CuCN + (CN)2
Dikyan lze také získat rozkladem kyanidu rtuťnatého:
Hg(CN)2 → Hg + (CN)2
Reference
- ↑ a b Cyanogen. pubchem.ncbi.nlm.nih.gov [online]. PubChem [cit. 2021-05-23]. Dostupné online. (anglicky)
Literatura
- VOHLÍDAL, Jiří; ŠTULÍK, Karel; JULÁK, Alois. Chemické a analytické tabulky. 1. vyd. Praha: Grada Publishing, 1999. ISBN 80-7169-855-5.
Externí odkazy
 Obrázky, zvuky či videa k tématu Dikyan na Wikimedia Commons
Obrázky, zvuky či videa k tématu Dikyan na Wikimedia Commons