Chlorid osmičitý
| Chlorid osmičitý | |
|---|---|
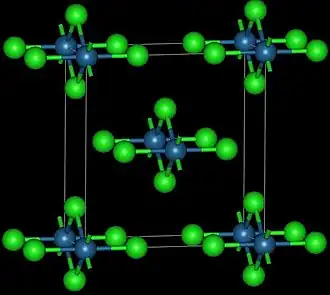 Krystalická struktura OsCl4 | |
| Obecné | |
| Systematický název | chlorid osmičitý |
| Ostatní názvy | osmium tetrachlorid |
| Anglický název | Osmium (IV) chloride |
| Německý název | Osmiumtetrachlorid |
| Sumární vzorec | OsCl4 |
| Vzhled | červeno-černé kosočtverečné krystaly |
| Identifikace | |
| Registrační číslo CAS | 10026-01-4 |
| Vlastnosti | |
| Molární hmotnost | 332,041 g/mol |
| Teplota tání | rozklad |
| Teplota rozkladu | 323 °C |
| Hustota | 4,380 g/cm3 |
| Rozpustnost ve vodě | rozpustný v organických rozpouštědlech |
| Struktura | |
| Krystalová struktura | kosočtverečná |
| Bezpečnost | |
 GHS06  GHS07 Nebezpečí[1] | |
Některá data mohou pocházet z datové položky. | |
Chlorid osmičitý (OsCl4) je anorganická sloučenina patřící mezi halogenidy s prvkem v oxidačním čísle IV.
Vytváří načervenalo-černé kosočtverečné krystaly, ve kterých jsou atomy osmia uspořádány do tvaru osmistěnu.[2]
Příprava
Chlorid osmičitý se připravuje rozpouštěním oxidu osmičelého v koncentrované kyselině chlorovodíkové (ta zde působí jako redukční činidlo):
OsO4 + 8 HCl → OsCl4 + 4 H2O + 2 Cl2.[3]
nebo zahříváním elementárního osmia při vysokém tlaku:
Os + 2 Cl2 → OsCl4.[4]
Reakce
Oxid osmičelý může být vytvořen oxidací chloridu osmičelého chlornanem sodným:
OsCl4 + 4 NaClO → OsO4 + 4 NaCl + 2 Cl2.[5]
Podobné sloučeniny
Odkazy
Externí odkazy
 Obrázky, zvuky či videa k tématu chlorid osmičitý na Wikimedia Commons
Obrázky, zvuky či videa k tématu chlorid osmičitý na Wikimedia Commons
Reference
V tomto článku byl použit překlad textu z článku Osmium(IV) chloride na anglické Wikipedii.
- ↑ a b Osmium tetrachloride. pubchem.ncbi.nlm.nih.gov [online]. PubChem [cit. 2021-05-23]. Dostupné online. (anglicky)
- ↑ Wells A.F. (1984) Structural Inorganic Chemistry 5th edition Oxford Science Publications ISBN 0-19-855370-6
- ↑ THORPE, Thomas Edward. A Dictionary of Applied Chemistry. [s.l.]: Longmans, Green, and Co., 2004. Dostupné online. S. 727.
- ↑ Chemistry: Periodic Table: Osmium: chemical reaction data [online]. WebElements [cit. 2008-06-27]. Dostupné online.[nedostupný zdroj]
- ↑ PATNAIK, Pradyot. Handbook of Inorganic Chemicals. [s.l.]: McGraw-Hill Professional, 2004. Dostupné online. ISBN 0070494398. S. 672.
Portály: Chemie