2-methoxyethanol
| 2-methoxyethanol | |
|---|---|
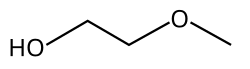 Strukturní vzorec | |
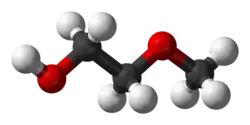 Model molekuly | |
| Obecné | |
| Systematický název | 2-methoxyethanol |
| Funkční vzorec | CH3OCH2CH2OH |
| Sumární vzorec | C3H8O2 |
| Vzhled | bezbarvá kapalina[1] |
| Identifikace | |
| Registrační číslo CAS | 109-86-4 |
| EC-no (EINECS/ELINCS/NLP) | 203-713-7 |
| PubChem | 8019 |
| ChEBI | 46790 |
| SMILES | COCCO |
| InChI | InChI=1S/C3H8O2/c1-5-3-2-4/h4H,2-3H2,1H3 |
| Číslo RTECS | KL5775000 |
| Vlastnosti | |
| Molární hmotnost | 76,094 g/mol |
| Teplota tání | −85 °C (188 K)[1] |
| Teplota varu | 124 °C (397 K)[1] |
| Hustota | 0,9647 g/cm3 (20 °C)[1] |
| Index lomu | 1,4024 (20 °C)[1] |
| Disociační konstanta pKa | 14,8[1] |
| Rozpustnost ve vodě | neomezeně mísitelný[1] |
| Rozpustnost v polárních rozpouštědlech | rozpustný v acetonu, ethanolu a dimethylformamidu[1] |
| Rozpustnost v nepolárních rozpouštědlech | rozpustný v diethyletheru a uhlovodících[1] |
| Tlak páry | 0,83 kPa (20 °C) 1,3 kPa (25 °C)[1] |
| Ionizační energie | 9,60 eV[1] |
| Povrchové napětí | 30,84 mN/m[1] |
| Termodynamické vlastnosti | |
| Standardní molární spalná entalpie ΔH°sp | −1673 kJ/mol[1] |
| Entalpie varu ΔHv | 594 J/g (25 °C) 493 J/g (124 °C)[1] |
| Bezpečnost | |
 GHS02  GHS07  GHS08 | |
| H-věty | H226 H302 H312 H332 H360 H370 H373[1] |
| P-věty | P203 P210 P233 P240 P241 P242 P243 P260 P261 P264 P270 P271 P280 P301+317 P302+352 P303+361+353 P304+340 P308+316 P318 P319 P321 P330 P362+364 P370+378 P403+235 P405 P501[1] |
| Teplota vzplanutí | 42 °C (315 K)[1] |
| Teplota vznícení | 285 °C (558 K)[1] |
Některá data mohou pocházet z datové položky. | |
2-Methoxyethanol je organická sloučenina patřící mezi glykolethery, se vzorcem C3H8O2, bezbarvá kapalina používaná hlavně jako rozpouštědlo. Jako i další glykolethery rozpouští mnoho různých druhů sloučenin a mísí se s vodou a řadou dalších rozpouštědel. Vyrábí se nukleofilní reakcí methanolu s protonovaným ethylenoxidem, následovanou přenosem protonu:
- C2H5O+ + CH3OH → CH3OCH2CH2OH + H+
2-methoxyethanol má jako rozpouštědlo využití v lacích, barvách, a pryskyřicích. Také se přidává do leteckých nemrznoucích směsí. V organokovové chemii jej lze použít na přípravu Vaskova komplexu a jiných podobných sloučenin, jako je karbonylchlorohydridotris(trifenylfosfin)ruthenatý komplex; při těchto reakcích slouží alkoholová skupina jako zdroj hydridových iontů a oxidu uhelnatého.
2-methoxyethanol poškozuje kostní dřeň a varlata. Vystavení této látce zvyšuje riziko granulocytopenie, makrocytické anémie, oligospermie, a azoospermie.[2]
Methoxyethanol se působením alkoholdehydrogenázy přeměňuje na kyselinu methoxyoctovou (methoxyacetát), která je vlastní příčinou jeho toxických účinků; následky otravy lze zmírnit ethanolem a kyselinou octovou. Methoxyacetát může vstupovat do Krebsova cyklu, kde vytváří kyselinu methoxycitronovou (methoxycitrát).[3]
Odkazy
Reference
V tomto článku byl použit překlad textu z článku 2-Methoxyethanol na anglické Wikipedii.
Externí odkazy
 Obrázky, zvuky či videa k tématu 2-methoxyethanol na Wikimedia Commons
Obrázky, zvuky či videa k tématu 2-methoxyethanol na Wikimedia Commons