1,2-Diaminopropan
| 1,2-diaminopropan | |
|---|---|
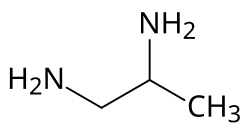 Strukturní vzorec | |
| Obecné | |
| Systematický název | propan-1,2-diamin |
| Funkční vzorec | CH3CH(NH2)CH2NH2 |
| Sumární vzorec | C3H10N2 |
| Vzhled | bezbarvá kapalina[1] |
| Identifikace | |
| Registrační číslo CAS | 78-90-0 |
| EC-no (EINECS/ELINCS/NLP) | 201-155-9 |
| PubChem | 6567 |
| SMILES | CC(N)CN |
| InChI | InChI=1S/C3H10N2/c1-3(5)2-4/h3H,2,4-5H2,1H3 |
| Vlastnosti | |
| Molární hmotnost | 74,125 g/mol |
| Teplota tání | −12 °C (261 K)[1] |
| Teplota varu | 119 °C (392 K)[1] |
| Hustota | 0,8584 g/cm3[1] |
| Index lomu | 1,446 |
| Rozpustnost ve vodě | rozpustný[1] |
| Tlak páry | 1,2 kPa (20 °C)[1] |
| Bezpečnost | |
 GHS02  GHS05  GHS07 Nebezpečí[1] | |
| H-věty | H226 H302 H312 H314[1] |
| P-věty | P210 P233 P240 P241 P242 P243 P260 P264 P270 P280 P301+312 P301+330+331 P302+352 P303+361+353 P304+340 P305+351+338 P310 P312 P321 P322 P330 P363 P370+378 P403+235 P405 P501[1] |
| Teplota vzplanutí | 33 °C (306 K)[1] |
| Teplota vznícení | 416 °C (689 K)[1] |
Některá data mohou pocházet z datové položky. | |
1,2-Diaminopropan (systematický název propan-1,2-diamin) je organická sloučenina se vzorcem CH3CH(NH2)CH2NH2, jedná se o nejjednodušší chirální diamin. Používá se jako bidentátní ligand v koordinační chemii.
Výroba a příprava
Průmyslově se 1,2-diaminopropan vyrábí aminolýzou 1,2-dichlorpropanu.[2]
- CH3CHClCH2Cl + 4 NH3 → CH3CH(NH2)CH2NH2 + 2 NH4Cl
Touto a podobnými reakcemi se z odpadních organochloridů získávají aminy za použití amoniaku.[2]
Racemický 1,2-diaminopropan lze rozdělit na jednotlivé enantiomery přeměnou na příslušné sodné soli kyseliny vinné. Po přečištění jejich diastereomerů lze získat diamin reakcí amonné soli s hydroxidem sodným.[3] K oddělení enantiomerů lze také použít kyselinu N-p-toluensulfonylaspartovou, N-benzensulfonylaspartovou nebo N-benzoylglutamovou.
Použití
1,2-diaminopropan se používá při výrobě ligandu salpn, používaného v motorových olejích jako aditivum, které zachytává ionty kovů a tím zamezuje jejich katalytickému působení.
Reference
V tomto článku byl použit překlad textu z článku 1,2-Diaminopropane na anglické Wikipedii.
- ↑ a b c d e f g h i j k l 1,2-Diaminopropane. pubchem.ncbi.nlm.nih.gov [online]. PubChem [cit. 2021-05-24]. Dostupné online. (anglicky)
- ↑ a b M. Bartkowiak; G. Lewandowski; E. Milchert; R. Pelech. Optimization of 1,2-Diaminopropane Preparation by the Ammonolysis of Waste 1,2-Dichloropropane. Industrial & Engineering Chemistry Research. 2006, s. 5681–5687. doi:10.1021/ie051134u.
- ↑ G. Romanowski; M. Wera. Mononuclear and dinuclear chiral vanadium(V) complexes with tridentate Schiff bases derived from R(−)-1,2-diaminopropane: Synthesis, structure, characterization and catalytic properties. Polyhedron. 2010, s. 2747–2754. doi:10.1016/j.poly.2010.06.030.
Externí odkazy
 Obrázky, zvuky či videa k tématu 1,2-Diaminopropan na Wikimedia Commons
Obrázky, zvuky či videa k tématu 1,2-Diaminopropan na Wikimedia Commons